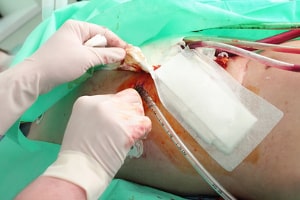
Seit dem 1. Januar 1995 ist der ordnungsgemäße Verkehr mit medizinischen Produkten im Medizinproduktegesetz (MPG) definiert. Dadurch soll sichergestellt werden, dass die zu verwendenden Produkte gewisse Standards erfüllen.
So dürfen sie beispielsweise weder die Sicherheit noch die Gesundheit der Patienten bzw. der Anwender gefährden. Außerdem müssen sie sich für den Sinn und Zweck eignen, der ihnen zugedacht ist.
Es muss sich demnach um unbedenkliche Produkte handeln, die keine oder zumindest einschätzbare Risiken bergen. Doch was qualifiziert Medizinprodukte überhaupt als solche und welche Anforderungen werden an sie gestellt? Wann ist ihre Nutzung gemäß Medizinproduktegesetz erlaubt und wann ist sie verboten? Welche Pflichten haben die Verantwortlichen zu erfüllen?
Wann der Vertrieb von Medizinprodukten gestattet ist, wann sie in Betrieb genommen werden dürfen, wieso die Klassifizierung der jeweiligen Produkte so wichtig ist, welche Behörden mit der Überprüfung der Produkte betraut sind und wie die Sanktionen aussehen, wenn gegen das Medizinprodukterecht verstoßen wird, können Sie in diesem Ratgeber nachlesen.
Inhalt
FAQ: Medizinproduktegesetz
Das Medizinproduktegesetz definiert den korrekten Umgang mit allen Medizinprodukten. Was darunter genau zu verstehen ist, lesen Sie hier.
Im Medizinproduktegesetz werden die Aufbewahrungspflichten nicht vorgegeben. diese befinden sich im der Medizinprodukteverordnung (MPV). Hier lesen Sie mehr dazu.
Verstöße gegen das Gesetz können entweder als Ordnungswidrigkeiten oder Straftaten geahndet werden und hohe Sanktionen nach sich ziehen.
Was sind Medizinprodukte?
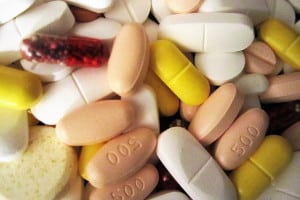
Im Medizinrecht wird zwischen Arzneimitteln und Medizinprodukten unterschieden. Letztere verfolgen eine medizinische Zweckbestimmung, sie werden demnach bei Menschen physikalisch angewandt. Arzneimittel hingegen wirken metabolisch (lassen eine Veränderung eintreten), immunologisch (stärken das Abwehrsystem) oder pharmakologisch (führen zu einer Wechselwirkung zwischen Arzneimittel und Körper).
Das Medizinproduktegesetz definiert medizinische Produkte in § 3 MPG wie folgt:
Medizinprodukte sind alle einzeln oder miteinander verbunden verwendeten Instrumente, Apparate, Vorrichtungen, Software, Stoffe und Zubereitungen aus Stoffen oder andere Gegenstände einschließlich der vom Hersteller speziell zur Anwendung für diagnostische oder therapeutische Zwecke bestimmten und für ein einwandfreies Funktionieren des Medizinproduktes eingesetzten Software, die vom Hersteller zur Anwendung für Menschen mittels ihrer Funktionen zum Zwecke
a) der Erkennung, Verhütung, Überwachung, Behandlung oder Linderung von Krankheiten,
b) der Erkennung, Überwachung, Behandlung, Linderung oder Kompensierung von Verletzungen oder Behinderungen,
c) der Untersuchung, der Ersetzung oder der Veränderung des anatomischen Aufbaus oder eines physiologischen Vorgangs oder
d) der Empfängnisregelungzu dienen bestimmt sind und deren bestimmungsgemäße Hauptwirkung im oder am menschlichen Körper weder durch pharmakologisch oder immunologisch wirkende Mittel noch durch Metabolismus erreicht wird, deren Wirkungsweise aber durch solche Mittel unterstützt werden kann.“
Medizinproduktegesetz: Welche Voraussetzungen müssen erfüllt sein?
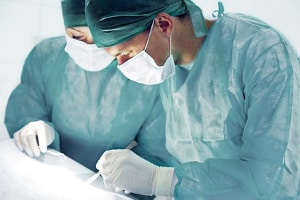
Die Anforderungen, die an Medizinprodukte gestellt werden, finden sich je nach Produkt im Anhang der jeweiligen Medizinprodukterichtlinie. Für aktive implantierbare Medizinprodukte gilt die Richtlinie 90/385/EWG, In-vitro Diagnostika sind in 98/79/EG geregelt und sonstige Medizinprodukte in 93/42/EWG.
Zudem sind der Verkehr mit Medizinprodukten und die Anwendung dieser laut Medizinproduktegesetz ausschließlich dann erlaubt, wenn sie eine sogenannte CE-Kennzeichnung aufweisen. „CE“ stammt unter anderem von „Comunidad Europea“ oder „Communauté Européenne“ und bedeutet „Europäische Gemeinschaft“. In den 1980er Jahren wurde aus diesem Grund in Deutschland von einem „EG-Zeichen“ gesprochen. 1993 wurde die offizielle Bezeichnung jedoch in „CE-Kennzeichnung“ geändert.
Mit einer solchen Kennzeichnung dürfen die Produkte nur dann versehen werden, wenn alle Voraussetzungen erfüllt wurden. Dies wird in einem sogenannten Konformitätsbewertungsverfahren überprüft. Eine CE-Kennzeichnung beweist demnach, dass alle gesetzlichen Bestimmungen eingehalten wurden.
Die klinische Bewertung muss entweder vom Hersteller selbst oder von einer „Benannten Stelle“, also einer akkreditierten Stelle, durchgeführt werden. Je nachdem, wie hoch die Risiken des jeweiligen Produktes sind, wird ein anderes Konformitätsbewertungsverfahren vorgenommen bzw. eine Benannte Stelle hinzugezogen.
Wie geht die Klassifizierung der Produkte vonstatten?
In § 13 geht es im Medizinproduktegesetz um die Klassifizierung medizinischer Produkte. Die Unterteilung aktiv implantierbarer Medizinprodukte in verschiedene Klassen richtet sich nach den Kriterien, die sich im Anhang IX der Richtlinie 93/42/EWG wiederfinden. Demnach existieren vier Klassen: I, IIa, IIb und III.
Für In-vitro Diagnostika gilt der Anhang II der Richtlinie 98/79/EG. Um das notwendige Konformitätsbewertungsverfahren hier auszuwählen, werden die Produkte ebenfalls in Klassen eingeteilt: Liste A, Liste B, Produkte zur Eigenanwendung und sonstige In-Vitro-Diagnostika.

Wie das jeweilige Bewertungsverfahren abzulaufen hat, ist in der Medizinprodukteverordnung (MPV) definiert. Diese ist jedoch nicht mit der gleichnamigen EU-Medizinprodukteverordnung gleichzusetzen. Diese EU-Verordnung über Medizinprodukte trägt im Englischen den Namen „Medical Device Regulation“ und wird daher mit MDR abgekürzt.
Welcher Anhang aus welcher Richtlinie Anwendung findet, ist demnach nicht in der Medizinprodukteverordnung der EU, sondern der nationalen Verordnung vermerkt. Das Medizinproduktegesetz soll wiederum dafür sorgen, dass die in den diversen Richtlinien genannten Vorschriften auch umgesetzt werden.
Welche Produkte müssen gemäß MPG einer speziellen Prüfung bzw. Bewertung unterzogen werden?
Es müssen laut MPG Produkte folgender Klassen durch eine Benannte Stelle überprüft werden:
Aktiv implantierbare Medizinprodukte:
- Klasse IIa
- Klasse IIb
- Klasse III
- steril in den Verkehr gebrachte Produkte (gemäß MPG) der Klasse I
- Produkte der Klasse I mit Messfunktion
In-vitro-Diagnostika:
- Liste A
- Liste B
- Produkte zur Eigenanwendung
Welche Benannte Stelle sich gemäß MPG der Zertifizierung annimmt, kann der Produkthersteller selbst entscheiden. Es muss jedoch eine Stelle sein, die in der jeweiligen Produktkategorie tätig ist und die Durchführung des entsprechenden Verfahrens übernehmen kann. Nur so kann sichergestellt werden, dass die Vorschriften aus dem Medizinproduktegesetz auch eingehalten wurden und weder Patient noch Anwender durch Medizinprodukte einer Gefährdung ausgesetzt werden.
Was ist laut Medizinproduktegesetz verboten?

Grundsätzlich sind gemäß MPG jegliche Medizinprodukte verboten, welche die Gesundheit oder die Sicherheit von Patienten, Anwendern oder anderweitig involvierten Personen trotz sachgemäßer Verwendung schädigen. Dies ist in § 4 MPG festgehalten. Das gleiche Verbot gilt für abgelaufene Produkte.
Wird ein Mangel oder Fehler an einem Produkt festgestellt, darf es nicht mehr verwendet werden. Handelt es sich um einen Fehler in der Gebrauchsanleitung eines medizinischen Gerätes oder am Gerät selbst, muss in der Regel das Bundesinstitut für Arzneimittel und Medizinprodukte bzw. das Paul-Ehrlich-Institut sowie der Hersteller davon in Kenntnis gesetzt werden.
Weiterhin heißt es im Medizinproduktegesetz, dass es verboten ist, medizinische Produkte in den Verkehr zu bringen, die eine Irreführung nach sich ziehen. Dies ist beispielsweise der Fall, wenn behauptet wird, dass ein Medizinprodukt
- gewisse Leistungen erbringen könnte, obwohl diese nicht der Wahrheit entsprechen,
- eine hundertprozentige Erfolgschance mit sich bringt oder
- auch nach längerem Gebrauch keinen Schaden anrichtet, obwohl dem so ist.
Doch in wessen Zuständigkeit fällt diese Irreführung? In § 5 MPG geht es um den Verantwortlichen für das „erstmalige Inverkehrbringen“ eines Medizinproduktes. Als solcher wird der Hersteller oder eine bevollmächtigte Person genannt. In der Gebrauchsanweisung des jeweiligen Produktes muss die Anschrift des Verantwortlichen in jedem Fall vermerkt sein.
Befindet sich das Medizinprodukt erst einmal im Verkehr, geht die Verantwortlichkeit bei der Inbetriebnahme sowie dem Betreiben des Produktes auf den jeweiligen Betreiber über. Dabei muss jedoch differenziert werden: Ein Betreiber ist nicht derjenige, der das medizinische Produkt oder Gerät nur bedient. Vielmehr handelt es sich dabei um denjenigen, der das Gerät besitzt und darüber bestimmt.
Was besagt das Medizinproduktegesetz bei Sonderanfertigungen?
In § 3 Nr. 8 MPG wird genau definiert, wann es sich um eine Sonderanfertigung handelt und wann nicht:
Sonderanfertigung ist ein Medizinprodukt, das nach schriftlicher Verordnung nach spezifischen Auslegungsmerkmalen eigens angefertigt wird und zur ausschließlichen Anwendung bei einem namentlich benannten Patienten bestimmt ist. Das serienmäßig hergestellte Medizinprodukt, das angepasst werden muss, um den spezifischen Anforderungen des Arztes, Zahnarztes oder des sonstigen beruflichen Anwenders zu entsprechen, gilt nicht als Sonderanfertigung.“
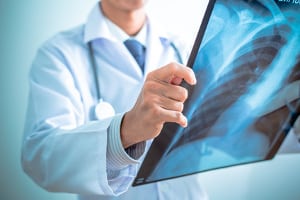
Es ist nicht verwunderlich, dass das Medizinproduktegesetz in einer Zahnarztpraxis ebenfalls beachtet werden muss. Ein geeignetes Beispiel, um gemäß MPG die Zulassung einer Sonderanfertigung zu verdeutlichen, ist der Zahnersatz. Dieser wird nicht nur nach speziellen Merkmalen hergestellt, sondern kann auch nur von der Person genutzt werden, für die er angefertigt wurde.
Da Zahnersatz zu Medizinprodukten der Klasse IIa gehört, muss das Konformitätsbewertungsverfahren von einer der akkreditierten Behörden durchgeführt werden. Weil es sich um eine Sonderanfertigung handelt, bedarf es außerdem einer sogenannten Konformitätserklärung. Der betroffene Patient muss durch diese zu identifizieren sein. Dies kann entweder durch seinen Namen, einen Code oder ähnliches geschehen.
Was besagt das Medizinproduktegesetz zu Aufbewahrungspflichten?
Die Vorschriften dazu, wie lange gewisse Dokumente, die im Zusammenhang mit Medizinprodukten stehen, aufbewahrt werden müssen, finden sich nicht im Medizinproduktegesetz, sondern in der Medizinprodukteverordnung (MPV).
§ 7 MPV Absatz 5 besagt dazu, dass die genannte Konformitätserklärung sowie die Dokumentation bei Sonderanfertigungen mindestens fünf Jahre aufbewahrt werden müssen. Handelt es sich um implantierbare Produkte, gilt sogar eine Aufbewahrungsfrist von 15 Jahren.

Auch das sogenannte Medizinproduktebuch, in dem Betreiber von Medizinprodukten jegliche Daten des Produktes dokumentieren müssen (§ 7 MPBetreibV), muss stets abrufbar und noch fünf Jahre gelagert werden, nachdem das jeweilige Produkt außer Betrieb genommen wurde. Wer bis 1998 ein sogenanntes Gerätebuch führte, konnte dieses in den darauf folgenden Jahren jedoch als Medizinproduktebuch weiterführen.
Um den Überblick über die aktiven nicht implantierbaren Medizinprodukte nicht zu verlieren, sieht § 8 MPBetreibV außerdem ein sogenanntes Bestandsverzeichnis vor. Laut MPG müssen zu jedem medizinischen Produkt folgende Angaben gemacht werden:
- Bezeichnung, Art und Typ, Loscode oder die Seriennummer, Anschaffungsjahr des Medizinproduktes,
- Name oder Firma und die Anschrift des für das jeweilige Medizinprodukt Verantwortlichen nach § 5 des Medizinproduktegesetzes,
- die der CE-Kennzeichnung hinzugefügte Kennnummer der Benannten Stelle, soweit diese nach den Vorschriften des Medizinproduktegesetzes angegeben ist,
- soweit vorhanden, betriebliche Identifikationsnummer,
- Standort und betriebliche Zuordnung,
- die vom Hersteller angegebene Frist für die sicherheitstechnische Kontrolle nach § 6 Abs. 1 Satz 1 oder die vom Betreiber nach § 6 Abs. 1 Satz 2 festgelegte Frist für die sicherheitstechnische Kontrolle.“ (§ 8 MPBetreibV)
Wie muss laut Medizinproduktegesetz eine Einweisung erfolgen?
Der Betreiber eines medizinischen Produktes hat laut Medizinproduktegesetz die Pflicht, sein Personal einzuweisen, bevor das Medizinprodukt verwendet wird. Dass eine Einweisung stattgefunden hat, muss außerdem belegt werden können. Dies sollte § 7 MPBetreibV zufolge durch ein Medizinproduktebuch geschehen.
Folgende Angaben müssen dokumentiert werden, um nicht gegen die Nachweispflicht aus dem Medizinproduktegesetz zu verstoßen:

- Name des Einweisers
- Befugnisse des Einweisers
- Namen der einzuweisenden Personen
- Angaben zum Medizinprodukt (Bezeichnung/Hersteller/Typ)
- Zeitpunkt der Einweisung
Übrigens: Befugte Personen sowie der Hersteller eines Produktes dürfen Anwender und beauftragte Personen mit dem jeweiligen Produkt oder Gerät vertraut machen. Beauftragte Personen jedoch haben lediglich das Recht, Anwender einzuweisen. Die Vorschriften zum Sicherheitsbeauftragten für Medizinprodukte finden sich im MPG in § 30. Alle Beteiligten müssen die Dokumentation der Einweisung zudem unterschreiben.
So werden Verstöße gegen das Medizinproduktegesetz geahndet
Wurde gegen das Medizinproduktegesetz verstoßen, können die Sanktionen unterschiedlich hoch ausfallen. Dies ist in einer Unterscheidung von Ordnungswidrigkeiten und Straftaten begründet. Als Ordnungswidrigkeit wird es beispielsweise gewertet, wenn eine CE-Kennzeichnung nicht wie vorgeschrieben angebracht wurde.
Ähnlich verhält es sich mit Medizinprodukten, die den Anforderungen aus dem Medizinproduktegesetz nicht entsprechen und trotzdem ausgestellt werden, ohne dass ein Schild oder ähnliches auf diesen Umstand hinweist. Laut MPG können Ordnungswidrigkeiten dieser Art mit einem Bußgeld von bis zu 25.000 Euro sanktioniert werden.
Anders verhält es sich bei Straftaten. Wird z. B. ein medizinisches Produkt in den Verkehr gebracht oder angewandt, welches den Vorschriften der Röntgenverordnung unterliegt oder bei dessen Herstellung Strahlung eingesetzt wurde, kann eine Geldstrafe oder eine Freiheitsstrafe von bis zu drei Jahren fällig werden. Wenn die Tat fahrlässig begangen wurde, kann sie laut Gesetz mit einer Freiheitsstrafe von bis zu einem Jahr bestraft werden.



 (55 Bewertungen, Durchschnitt: 4,65 von 5)
(55 Bewertungen, Durchschnitt: 4,65 von 5)
Hallo, wenn wir ein Medizinprodukt (in unserem Fall eine FFP MAske vertreiben) gibt es eine Vorlage zur Dokumentationspflicht für einen solchen Vertrieb. Einen MPG Beauftragten haben wir selbstverständlich.
Danke und Viele Grüße
Interessant, dass medizinische Produkte gewisse Standards erfüllen müssen und beispielsweise weder die Gesundheit noch Sicherheit des Patienten gefährden dürfen. Bevor ich einen Hersteller deswegen verklage, werde ich mich an eine Anwältin für Medizinrecht wenden. Damit bin ich dann auf der sicheren Seite und werde den Prozess hoffentlich gewinnen.
Welche Pflichten entstehen einem niedergelassenen Arzt aus diesem Gesetz.
Was prüft das Gewerbeaufsichtsamt?